01 焦耳-汤姆孙效应的初步解释
- 1mol 由

讯享网到 ,外界做功得:
,外界做功得:
- 一般情况下,内能是温度和体积的函数
- 根据

- 有

- 有
- 若是理想气体

- 理想气体内能只与温度有关

- 可得

- 这表明:理想气体没有焦耳 汤姆孙效应
- 对于实际气体,若考虑到分子间存在斥力,但是忽略分子间的引力
- 有范德瓦尔斯方程


- 可得
![(C_{V,m}+R)(T_{2}-T_{1})=b(p_{1}-p_{2})+[E_{1}-E_{2}]](https://51itzy.com/uploads/202412/23/d8d6e00325d3a7fb.jpg)
- 这表明当范德瓦尔斯方程中主要考虑斥力作用时,表现出负的焦耳-汤姆孙效应
- 也表明当范德瓦尔斯方程中主要考虑引力作用时,表现出正的焦耳-汤姆孙效应
- 有范德瓦尔斯方程
02 焚风
- 气流上升缓慢,干燥的空气导热性很差,该过程可被视为准静态绝热过程
- 厚度为dz的一薄层大气,在单位面积上由静力平衡得:
- n是单位体积内气体分子的个数
- 可得

- 对于绝热过程

- 有



- 有
- 由理想气体物态方程得
- 绝热过程

 表示水的汽化热
表示水的汽化热 表示气团中水蒸气的摩尔数
表示气团中水蒸气的摩尔数- 联立得

- 最后导出饱和大气的绝热递减率
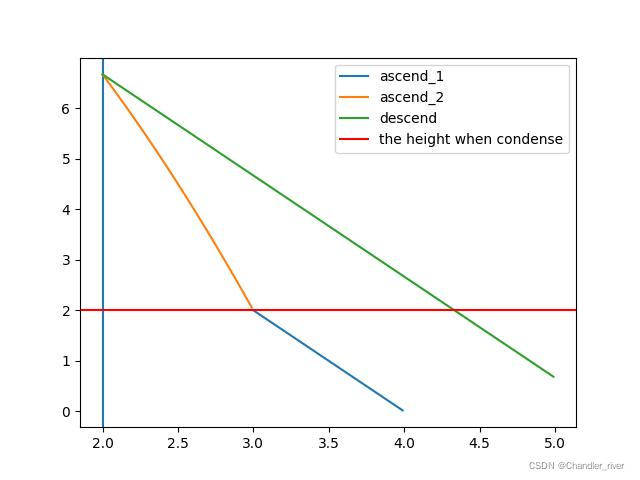
由于水蒸气的凝结,水蒸气的量会随着高度的增加而减少,于是 ,因此饱和大气的绝热递减率的绝对值比干燥大气的绝热递减率的绝对值要小,即潮湿空气的温度随高度的升高减小得要慢一些,对于潮湿空气,由于在温度降低时可能释放汽化热,故平均涞水,每上升1km,温度降低6.5K。
,因此饱和大气的绝热递减率的绝对值比干燥大气的绝热递减率的绝对值要小,即潮湿空气的温度随高度的升高减小得要慢一些,对于潮湿空气,由于在温度降低时可能释放汽化热,故平均涞水,每上升1km,温度降低6.5K。
爬坡气团的温度变化(示意图)

03 麦克斯韦分布律
- 范德瓦尔斯方程

- 速率分布函数
 的物理意义
的物理意义
- 速率分布在
 附近的单位速率间隔中的分子数占总分子数的百分比
附近的单位速率间隔中的分子数占总分子数的百分比 - 此时满足

- 做球坐标变换得


- 这表明,速率相同的粒子数目与粒子方向无关
- 速率分布在
- 做如下变换


- 解一个微分方程
- 两个条件
- 1.归一化,即

- 得

- 得
- 2
- .

- 1.归一化,即
- 最终可得
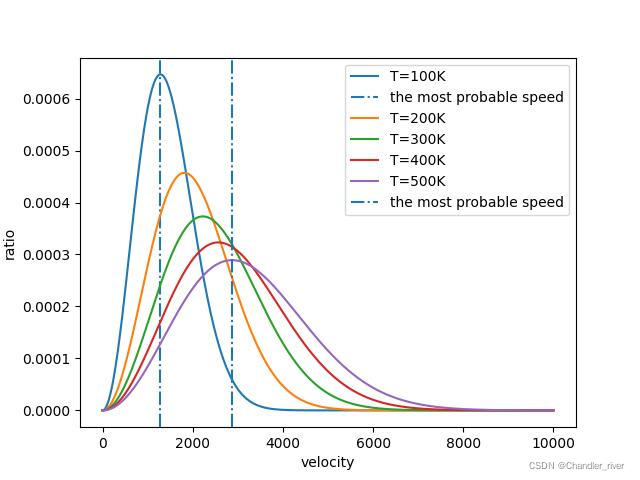
- 图像
import matplotlib.pyplot as plt import math import random def draw(T): m = 1.674 * 10 (-27) k = 1.38 * 10 (-23) T = T a = [i*0.01 for i in range(0,)] f = lambda x:4*math.pi*(m/(2*math.pi*k*T))(1.5)*math.e((-(m*x2)/(2*k*T)))*x2 b = [f(i) for i in a] plt.plot(a,b,label="T="+str(T)+"K") axv = (2*k*T/m)0.5 if random.choice([0,1]): plt.axvline(axv,linestyle="-.",label="the most probable speed") t = [100,200,300,400,500] for i in t: draw(i) plt.legend() plt.xlabel("velocity") plt.ylabel("ratio") plt.savefig("2.jpg")
讯享网
04 理想气体的摩尔热容
- 非高温下,不考虑振动状态
- 振动能级之间的能量间隔较大,一般在常温下分子的振动状态不会发生显著改变,因此对热容的贡献可以忽略
-
- 单原子理想气体的等体摩尔热容

- 双原子理想气体的等体摩尔热容

- 非线性的多原子分子的等体摩尔热容

- 单原子理想气体的等体摩尔热容
- 经典的能量均分原理
- 一个分子的平动能、转动能和振动能的表达式中的每一个平方项称为一个自由度
- 能量均匀地分配在每一个自由度,数值上为

- 一个分子有t个平动自由度,r个转动自由度和s个振动自由度
- 振动方式有两个平方项(振动动能,振动势能)

版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌侵权/违法违规的内容,请联系我们,一经查实,本站将立刻删除。
如需转载请保留出处:https://51itzy.com/kjqy/67203.html