今天给同学们分享一篇实验文章“Efficient in vivo genome editing prevents hypertrophic cardiomyopathy in mice”,这篇文章发表在Nat Med期刊上,影响因子为82.9。
结果解读:
双AAV9编码的基因编辑器和原始空间设计
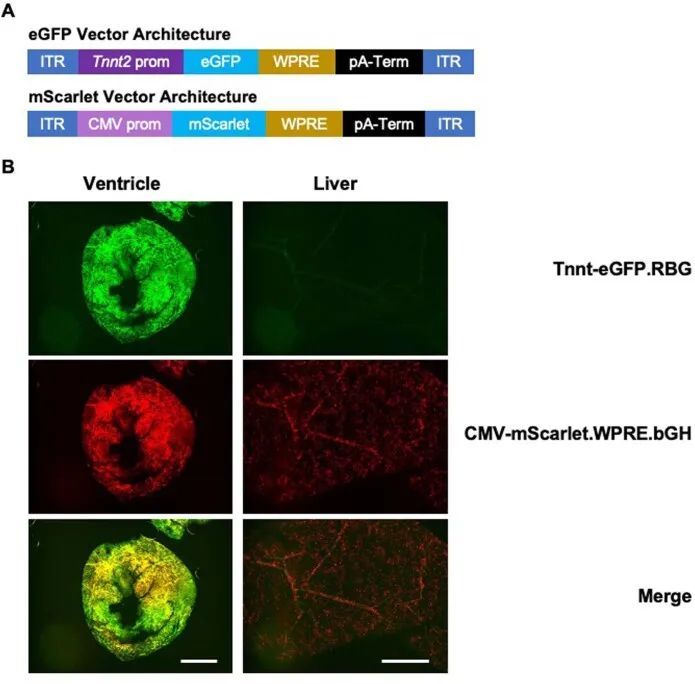
作者采用了分裂内源子设计,需要共转导两个AAV载体,每个载体分别表达基因编辑酶的一半,并通过转剪重组在细胞内重构完整长度的基因编辑酶。为了评估双AAV9感染心肌细胞的毒性和效率,作者进行了试验,使用了两个AAV9病毒,分别在Tnnt2启动子下表达eGFP荧光标记物 14 ,或在广泛表达的CMV启动子下驱动mScarlet荧光标记物(扩展数据图1a)。接受每个载体每千克体重3×10 13 载体基因组的胸腔内注射的野生型(WT)小鼠具有正常的生命力和存活率。注射后3周收集的组织显示正常的组织学结构,并且心脏中有明显的双重荧光信号,但肝脏中没有(扩展数据图1b)。
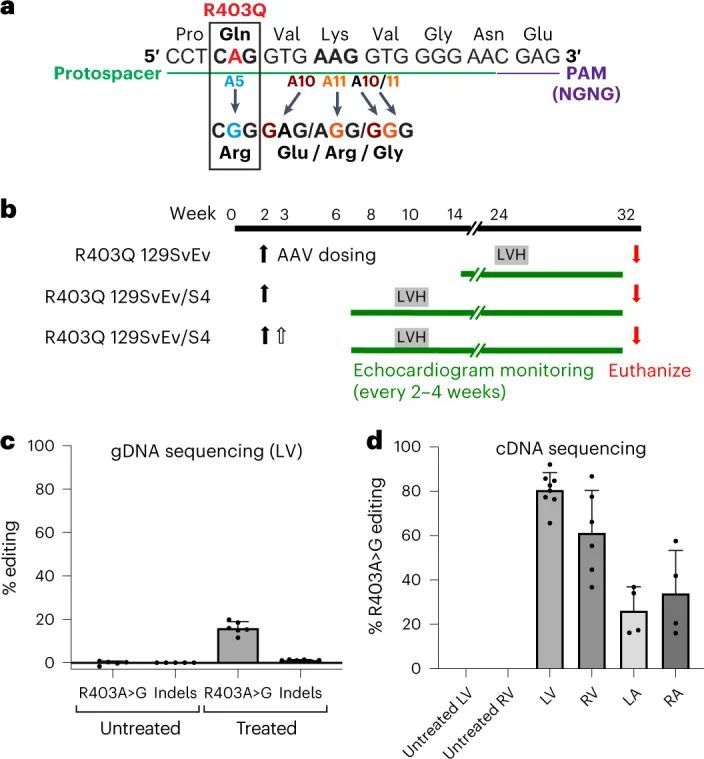
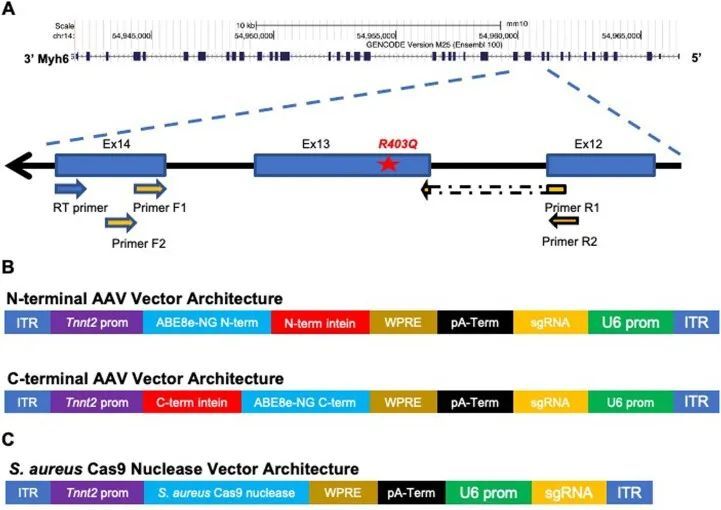
致病变异体R403Q是由G>A转换引起的(扩展数据图2a),是ABE的目标。作者使用了特别活跃的脱氨酶ABE8e,并设计了一个原始空间序列,将R403Q变异体放置在A5位置(从原始空间序列的PAM远端计数)(图1a)。这个单导RNA(sgRNA)使用附近的“CGAG”PAM,被一种作者选择的链球菌喉炎链球菌Cas9变体SpCas9-NG高效识别,用于碱基编辑。作者将碱基编辑器的每个半部分与Tnnt2启动子控制下的相同sgRNA一起引入双AAV9中(扩展数据图2b)。
两个HCM小鼠模型的基因编辑和体内监测
作者在两株小鼠系中针对R403Q变异体进行了研究(图1b)。R403Q-129SvEv雄性小鼠在20-25周龄时发展出LVH,从而模拟人类患者中潜在的HCM发作。R403Q-129SvEv/S4杂交小鼠是由偶然的R403Q-129SvEv和129S4交配产生的,雄性和雌性小鼠在8-10周龄时迅速发展出LVH,从而模拟具有急性HCM的患者。
基因编辑可以预防心脏纤维化
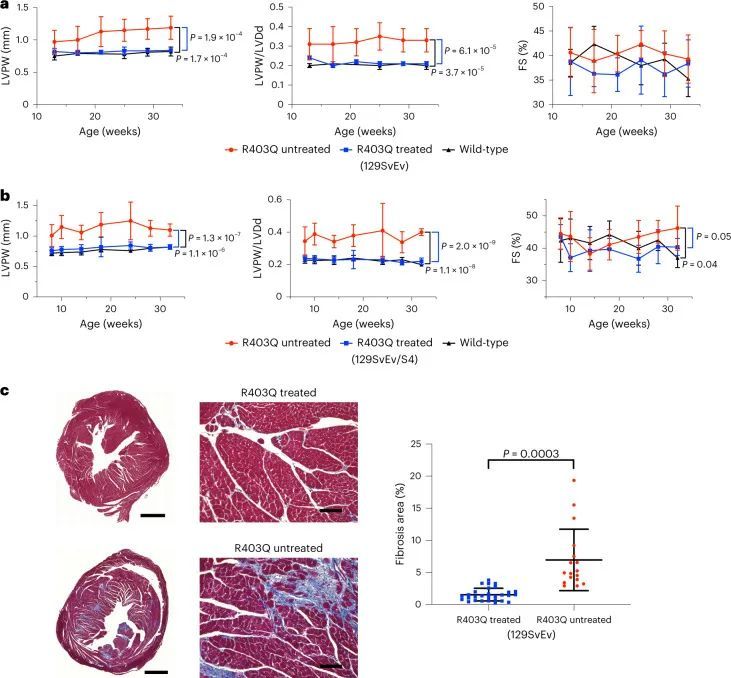
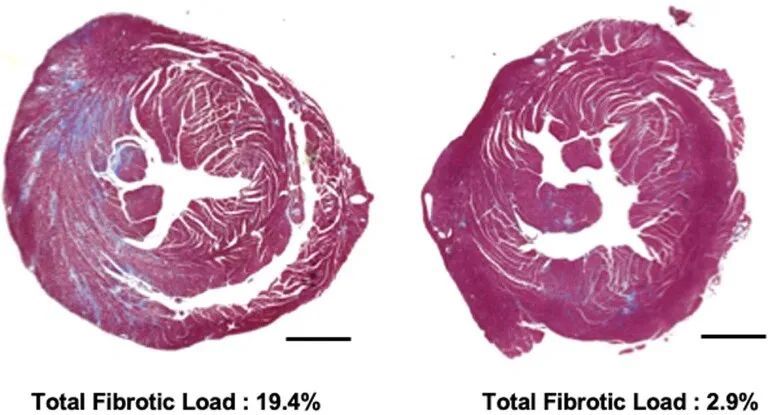
心肌纤维化在HCM小鼠模型中明显增加。在人类患者中,纤维化导致不良结果,包括心力衰竭和心律失常。作者研究了WT小鼠和经过处理和未经处理的R403Q-129SvEv小鼠(34周龄)的心室切片的显微镜心脏组织学,以确定编辑对心肌纤维化的影响(图2c和扩展数据图3)。与以前的研究类似,未经处理的R403Q-129SvEv小鼠相比,WT小鼠显示出更多的局灶性和弥漫性纤维化。经过处理的小鼠的纤维化程度与WT小鼠相似,显著少于未经处理的小鼠(P = 0.0003)。
旁观者编辑和组织病理学评估
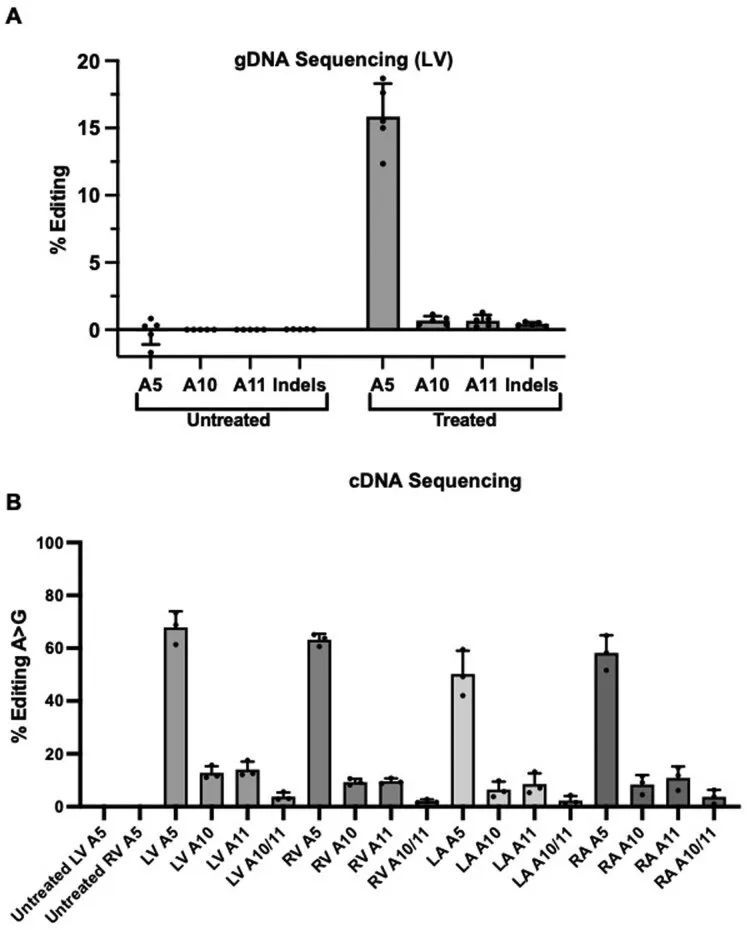
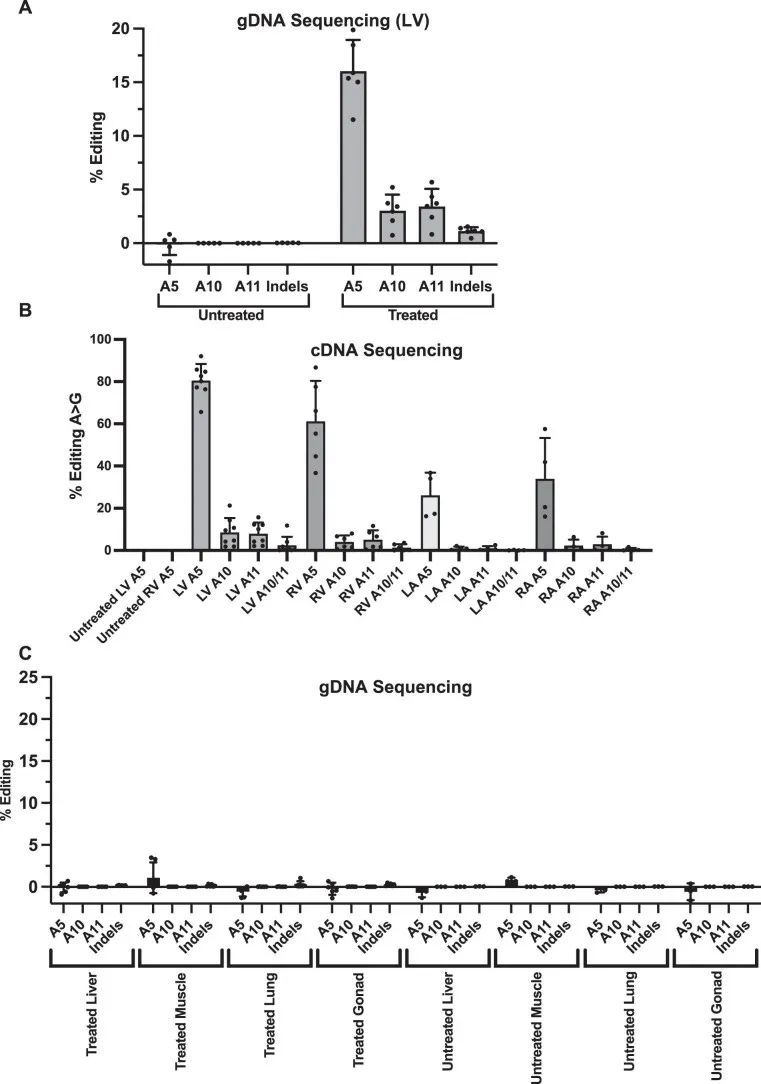
作者评估了碱基编辑的R403Q小鼠中旁观者突变的频率,因为氨基酸替代可能是有害的。使用从处理过的R403Q-129SvEv小鼠的心脏组织中提取的gDNA和RT-PCR扩增的Myh6 mRNAs,作者确定了旁观者腺嘌呤残基在原始空间序列位置10和11处的编辑(图1a),以及插入缺失的引入。平均而言,最常见的旁观者编辑在gDNA中为3.4% ± 1.7%,在RNA中为5.0% ± 4.8%(扩展数据图4a,b);观察到很少的插入缺失(<2%)。在保持致病性R403Q的等位基因中没有发生旁观者编辑。此外,序列数据表明适当编辑A5致病性核苷酸和旁观者编辑的比例之间存在相关性:A10:r = 0.68,P = 2 × 10 −12 ;A11:r = 0.45,P = 2 × 10 −5 。
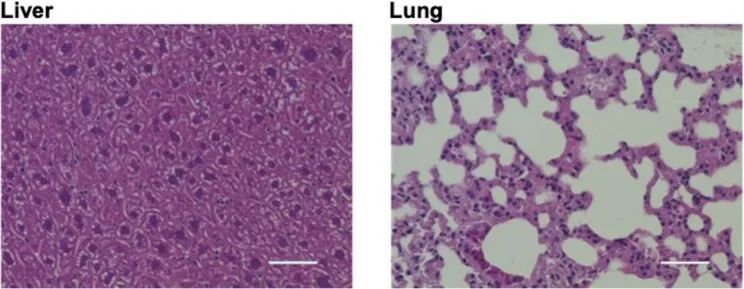
作者还比较了来自LVs、肝脏、骨骼肌、肺和生殖腺的R403Q-129SvEv小鼠中gDNA的靶向(A5)和旁观者编辑(扩展数据图4c)。观察到非常低水平的靶向编辑,并且在非心脏组织中几乎没有旁观者编辑发生,与Tnnt2启动子的心肌细胞特异性表达一致。
对两剂基因编辑器AAV9的评估
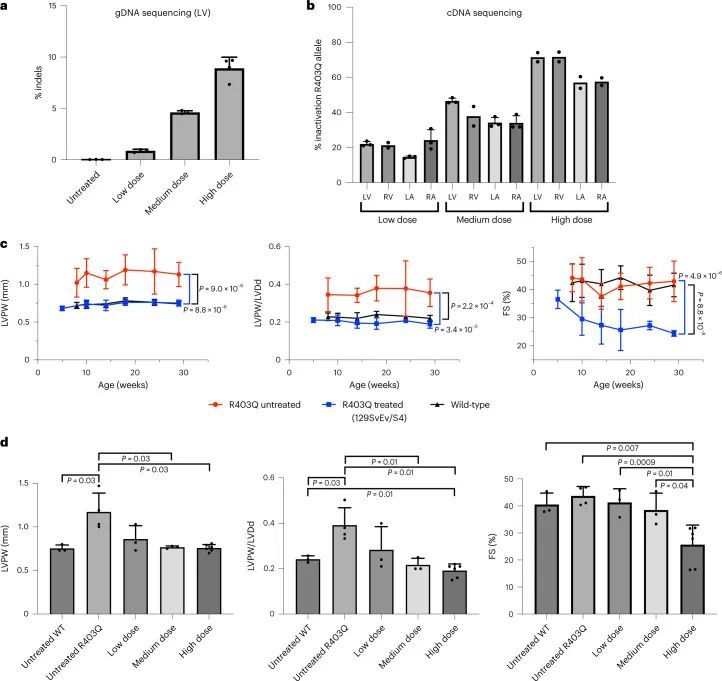
尽管单次注射携带ABE8e的双重AAV9能够阻止所有接受治疗的R403Q小鼠发展HCM,但编辑效率在小鼠之间存在差异,并且在右心室和心房组织中较左心室低(图1d)。由于HCM可以导致右心室和心房发生病理性重塑,作者测试了第二剂双重AAV是否能够改善这些心腔的编辑效果。由于在小鼠中,当两剂AAV9在接近的时间点和新生儿第14天之前注射时不会引发免疫反应(参考文献2),作者在R403Q-129SvEv/S4小鼠的第一剂注射后的1周内进行了第二剂注射(图1b)。
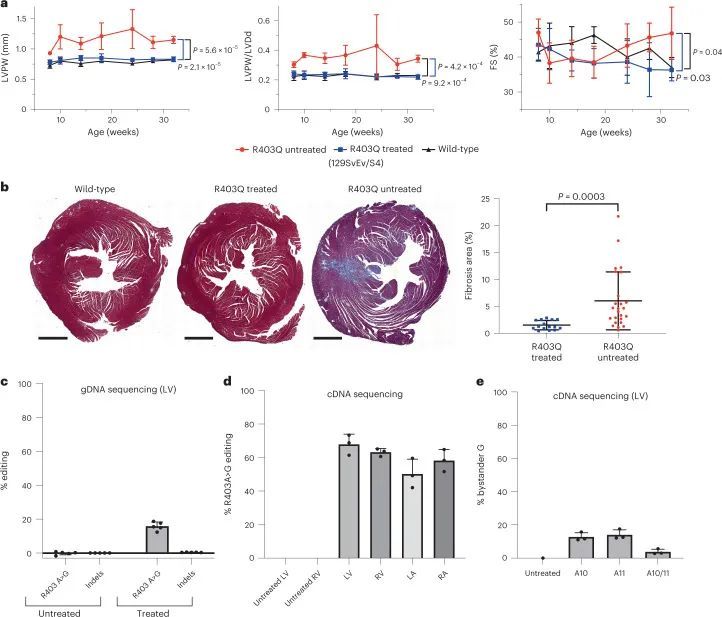
意外的是,额外的剂量并没有显著增加LV和RV的平均编辑效率(图3c,d)。对LV gDNA的分析显示,两剂量时的编辑率为15.8% ± 2.5%(图3c和扩展数据图6a),而一剂量时的编辑率为16.0% ± 2.9%(图1c和扩展数据图4a)。RNA分析显示,LV和RV在两剂量和一剂量后的编辑效率相似(LV:68% ± 6%对81% ± 8%;RV:63% ± 2%对61% ± 19%)。相比之下,心房的编辑效率在两剂量时比一剂量时有所提高(LA:50% ± 9%对26% ± 11%,P = 0.02;RA:58% ± 7%对34% ± 19%,P = 0.08)(图1d和图3d)。

R403Q修正使转录组恢复正常
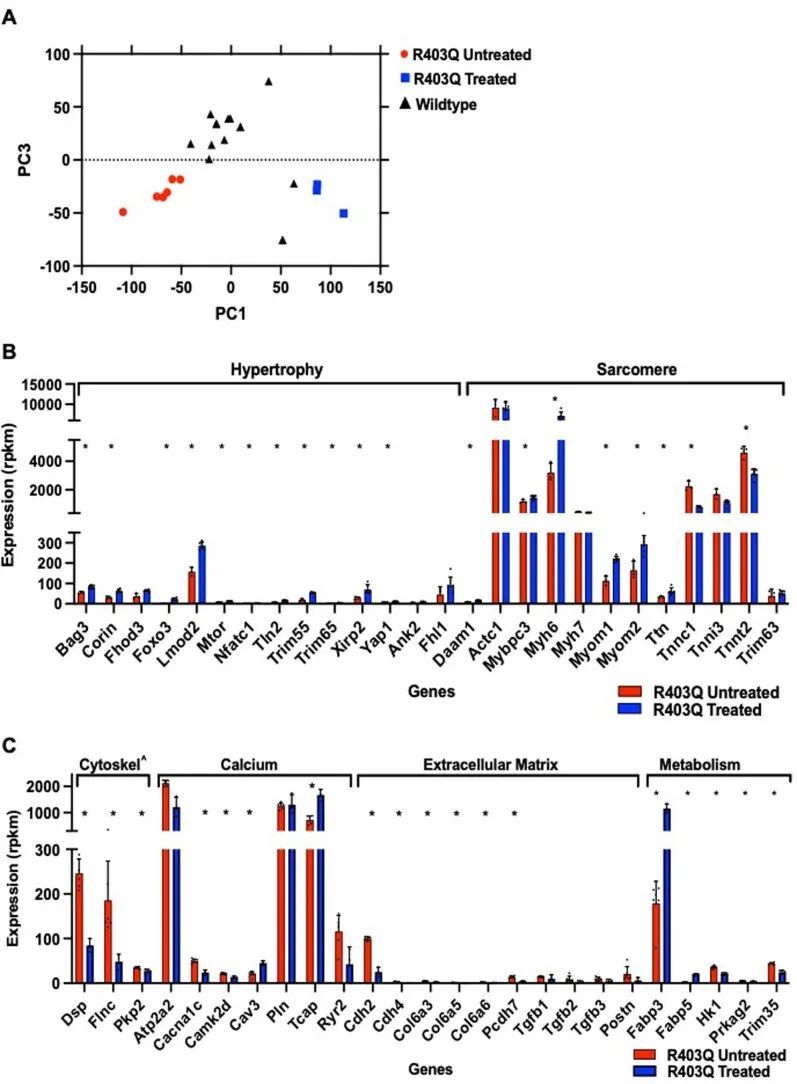
作者通过RNA测序(RNA-seq)分析(方法)评估了来自WT、未经处理和经过处理的R403Q-129SvEv/S4小鼠的LV组织的转录反应(扩展数据图7)。主成分分析比较所有表达的转录本(任何组中具有≥3 RPKM表达的n = 12,035个RNA)显示,与未经处理的R403Q-129SvEv/S4小鼠相比,WT和经过处理的小鼠之间的相似性更大。主成分1和3分别解释了WT和R403Q-129SvEv/S4之间25%和12%的方差(扩展数据图7a)。然后,作者有选择地比较了在小鼠模型和患有HCM的人患者中已知参与肥厚重塑的转录本。尽管同一治疗组中的小鼠基因表达有所变化,但总体上转录水平的平均倍数变化与未经处理的小鼠相比,表明机械工作、代谢应激和细胞外基质扩张更大。未经处理的小鼠表达了更高水平的编码收缩蛋白(Myh7、Mybpc3、Myom1、Myom2和Ttn)的转录本,与肥大生长(Ank2、Daam1、Fhl、Trim 63和Yap)相关,并使代谢从正常脂肪酸利用(Fabp,在处理过的小鼠中较高)转向糖酵解(mTOR、Prkag2和HK1)。与组织病理学发现一致(图2c和3b),未经处理的小鼠中纤维生成基因(Col6a5、Col6a6、Postn、Tgfb2和Ctgf)的表达较高。
基因组范围的离靶编辑评估
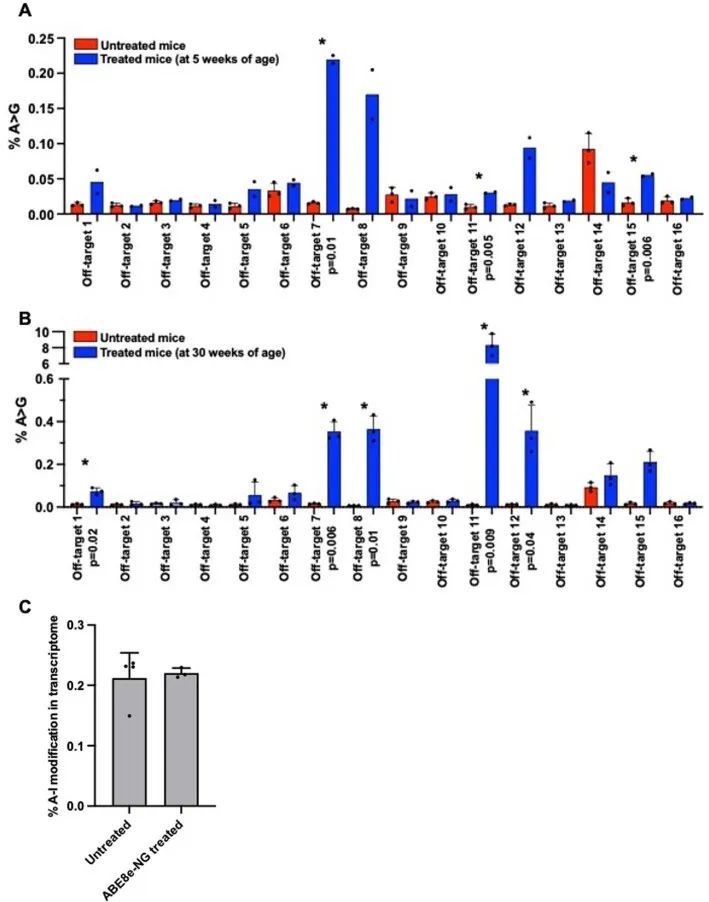
与旁观者编辑(靠近目标核苷酸)不同,离靶编辑是指ABE8e与与引导序列同源的不同基因组位点结合。作者使用CIRCLE-seq技术鉴定可能的全基因组离靶位点(扩展数据图8),这些位点可能被sgRNA-SpCas9-NG复合物结合。在从基因组LV DNA中扩增潜在的离靶编辑位点后,作者进行了下一代测序分析。许多被鉴定出的顶级位点位于重复序列中,作者无法特异性地通过PCR扩增来评估编辑情况,但作者认为在这些重复序列中的离靶编辑不太可能对健康产生不利影响。在成功扩增的16个潜在离靶位点中,5周龄治疗小鼠中有3个位点发生了低(<0.25%)但具有统计学意义的编辑(扩展数据图8a)。对30周龄治疗和未治疗小鼠的分析结果(扩展数据图8b)显示,编辑发生率为8.3% ± 1。1%的A>G编辑发生在离最近的预测基因(Gm26107)未知功能的染色体3区域的离靶位点11上,该区域距离最近的基因约26 kb。其他四个被测试的位点位于离靶或内含子区域,其离靶编辑率较低但在统计学上具有显著意义(每个位点均小于0.4%)。
评估整个转录组的编辑情况
细胞RNA是ABE8e的已知底物,在将ABE8e脂质体转染到HEK293T细胞后,已报道出现了非靶向RNA编辑。作者通过对经过处理和未经处理的R403Q小鼠的LV RNA-seq数据中A到I核苷酸变化的定量分析来评估非靶向RNA编辑。与之前对编码持续表达ABE的AAV载体治疗动物的分析类似,处理和未处理小鼠中A到I RNA核苷酸变化的频率没有显著差异(扩展数据图8c)。
使用Cas9核酸酶消除突变等位基因以预防HCM
由于RNAi在小鼠中选择性地沉默R403Q转录本,并且在大约6个月内阻止了HCM的发展而没有不良后果,作者探索了使用碱基编辑器永久失活突变等位基因的效果。这种策略可以克服需要设计碱基编辑器来特异性修复每个致病变异的需求,通过编辑常见的良性多态性以产生等位特异性的移码失活。此外,人类基因组数据表明,在一个肌球蛋白等位基因中丧失功能变异是可以容忍的(MYH7 pLI = 0),在小鼠和人类中,正常肌球蛋白基因剂量的一半似乎足够维持正常心脏功能。
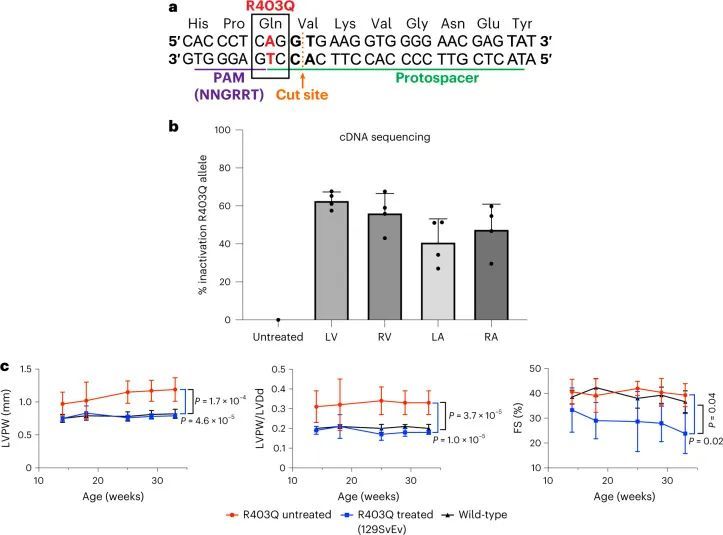
在将AAV9-Cas9核酸酶(1.1 × 10 13 vg kg −1 )经胸腔注射给R403Q-129SvEv小鼠(n = 5)(图 (图1b)1b),作者通过RT-PCR扩增LV RNA并进行高通量测序分析来评估R403Q等位基因的失活情况。由于大多数从indel等位基因转录的mRNA经历了无义介导的降解,因此只有少数转录本包含了移码突变。因此,作者计算R403Q等位基因失活的百分比为(1 - (R403Q读数总数除以WT读数总数))乘以100。
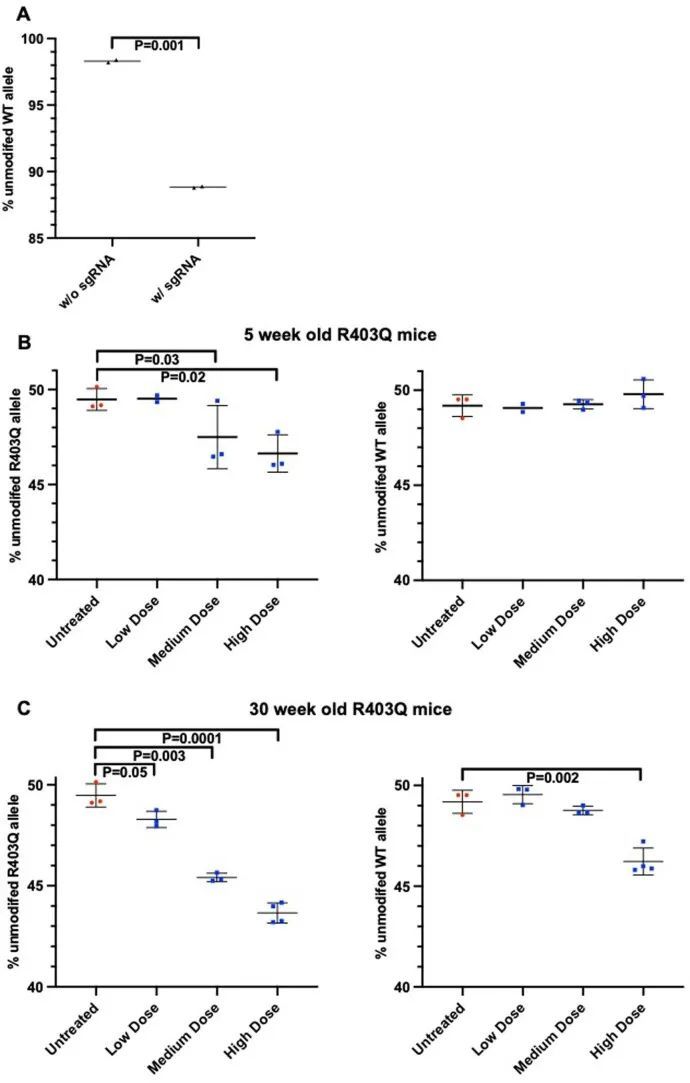
从这些数据中,作者推断出在接受高剂量AAV9-Cas9核酸酶和靶向sgRNA的杂合R403Q小鼠中,心脏功能障碍可能反映了对野生型等位基因的意外干扰。这种情况可能导致半合子R403Q心肌细胞的收缩性能严重下降,类似于带有纯合R403Q等位基因的小鼠,它们在新生儿时期就会死亡。或者,野生型等位基因的同时干扰和R403Q等位基因中插入缺失可能会消除Myh6表达并导致心肌细胞的死亡。
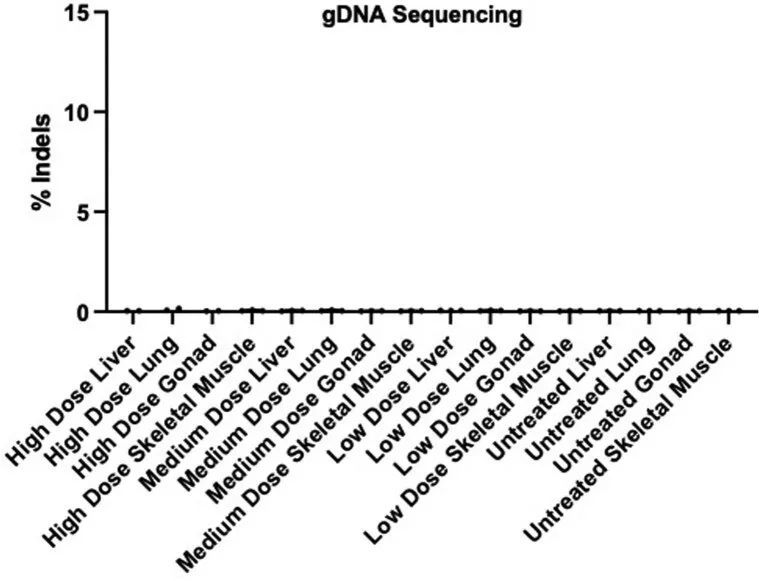
对LV gDNA的分析还表明,Cas9核酸酶会导致时间相关的显著且剂量依赖的WT等位基因丧失(扩展数据图9b,c)。在5周时收集的组织中,任何测试剂量下的小鼠都没有丧失WT等位基因,尽管中等或高剂量下R403Q等位基因的丧失是明显的。在30周时对治疗小鼠的分析显示,AAV9-Cas9的高剂量导致WT等位基因丧失约4%,相当于约8%的细胞等位基因丧失。由于心肌细胞约占心脏细胞的25%,且核酸酶表达仅限于心肌细胞,作者估计在接受高剂量AAV9-Cas9治疗的小鼠中,约有32%的心肌细胞携带破坏的WT Myh6等位基因。在接受高剂量AAV9-Cas9治疗的动物的肝脏、肺、生殖腺和骨骼肌中没有观察到Myh6的破坏(扩展数据图10)。
总结
总之,作者在哺乳动物模型中建立了碱基编辑器和Cas9核酸酶干预预防HCM的治疗窗口、风险和机会。这些可以形成一次性治疗心肌病的基础。对这篇文章的思路感兴趣的老师,欢迎咨询!


版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌侵权/违法违规的内容,请联系我们,一经查实,本站将立刻删除。
如需转载请保留出处:https://51itzy.com/kjqy/27289.html