一、制冷剂的相态变化
众所周知,物质有三种状态,就是固态、液态和气态。通常我们把固态的物体叫固体,固体物质内部的分子成有规则的布置,并在一定的晶格节点上振动。液态的物体叫液体,液态物质的分子彼此密集,相对地说是不可压缩,并具有相互移动位置的趋势。气态的物体叫气体,气态物质的分子处于不规则的运动中,其密度甚小,分子之间有一定的空隙,可以压缩,又能均匀地充满任何形状的空间。物质的三种状态,在一定的压力和温度条件下是可以相互转化的。其转化过程分别称为:
1.汽化,物质从液态转变为气态的过程称为汽化。
汽化有蒸发和沸腾两种形式。其中,在液体表面进行的汽化过程叫蒸发,在液体内部产生气泡的剧烈汽化过程叫沸腾。在一定压力下,蒸发在任何温度下都可进行,而沸腾只有液体被加热到一定温度才开始进行。当汽液两相共存并且保持平衡状态时称为饱和状态。此时的蒸汽和液体分别叫做饱和蒸汽和饱和液体,处于饱和状态的压力与温度称为饱和压力与饱和温度。饱和压力与饱和温度总是相互对应的,即一定的饱和压力对应着一定的饱和温度,反之亦然。二者之间的对应关系是:饱和温度愈高,饱和压力也愈高。反之,饱和压力愈高,饱和温度也愈高。这是饱和状态的一个重要特点。
2.冷凝,物质从汽态转变为液态的过程称为冷凝或叫做液化。
汽体的液化温度与压力有关,增大压力,可使汽体在较高的温度下液化。液化的基本方法是降低温度和增加压力。
3.升华,物质由固态直接转变为气态的过程称为升华。
4.凝华,物质由气态直接转变为固态的过程称为凝华。例如空气中的水蒸汽在膨胀阀上结霜时发生的过程。
二、制冷剂的压—焓图及热力性质表
制冷剂的热力状态可以用其热力性质表来说明(常用制冷剂的饱和热力性质表见附表),也可以用压-焓图来表示。压-焓图(lgP-h 图)是一种以绝对压力的对数值lgP 为纵坐标,焓值为横坐标的热工图表。采用对数值lgP(而不采用P)为纵坐标的目的是为了缩小图的尺寸,提高低压区域的精确度,但在使用时仍然直接从图上读出P的数值即可。
1.压-焓图(lgP-h图)的结构
压-焓图中有两条比较粗的曲线,左边一条为饱和液体线(干度χ=0),右边一条为干饱和蒸汽线(干度χ=1),两线交于一点K,且将图分成了三个区域。其中K 称为临界点,饱和液体线左侧为过冷液体区,干饱和蒸汽线右侧为过热蒸汽区,两线之间为湿蒸汽区。
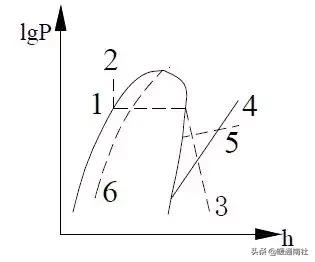
压—焓图中有六种等状态参数线,如图2-3 所示:
①等压线P:水平细直线。
②等焓线h:竖直细直线。
③等温线t:点划线,其在过冷液体区为竖直线,在湿蒸汽区为水平线,在过热蒸汽区为稍微向右下方弯曲的曲线。
④等熵线S:为从左到右稍向上弯曲的实线。
⑤等比容线υ:在湿蒸汽区和过热蒸汽区中,为从左到右稍向上弯曲的虚线,但比等熵线平坦,液体区无等比容线,因为不同压力下的液体容积变化不大。


版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌侵权/违法违规的内容,请联系我们,一经查实,本站将立刻删除。
如需转载请保留出处:https://51itzy.com/kjqy/65083.html